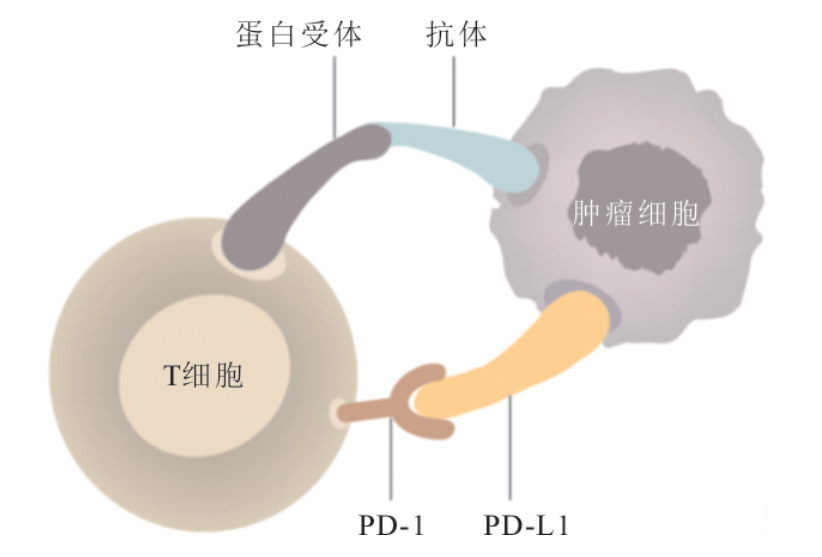
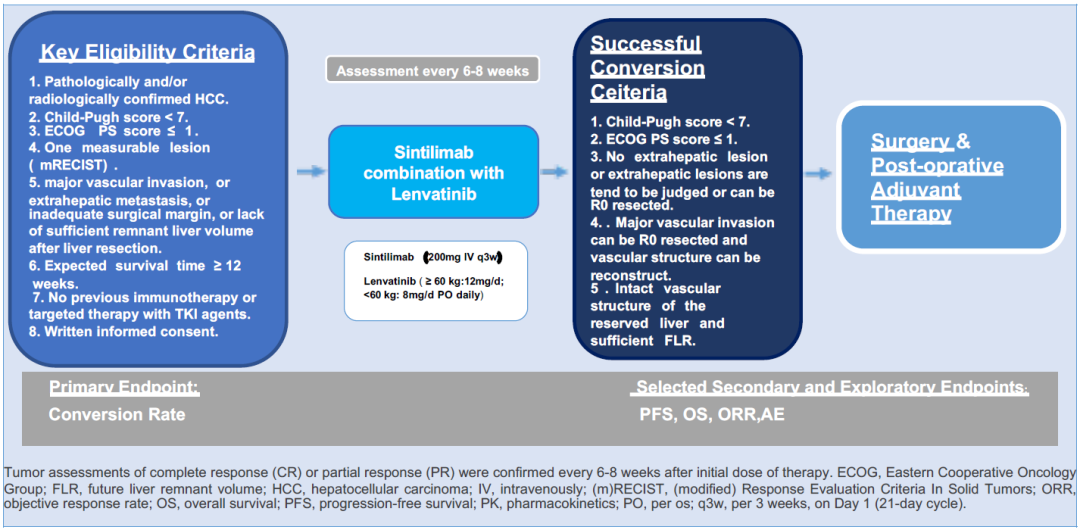
礼来制药(纽约证券交易所代码:LLY)和信达生物制药集团(香港联交所股票代码:01801)共同宣布,由双方联合开发的创新药物PD-1抑制剂达伯舒®(信迪利单抗注射液)获得中国国家药品监督管理局(NMPA)批准,联合贝伐珠单抗、培美曲塞和顺铂,用于经表皮生长因子受体酪氨酸激酶抑制剂(EGFR-TKI)治疗失败的EGFR基因突变阳性的局部晚期或转移性非鳞状非小细胞肺癌(NSCLC)患者的治疗。达伯舒®(信迪利单抗注射液)成为全球首个获批用于经EGFR-TKI治疗失败的EGFR阳性非鳞状非小细胞肺癌的PD-1抑制剂,实现了EGFR阳性非鳞状非小细胞肺癌在免疫治疗领域的“零突破”。 截至第二次期中分析,在意向治疗(ITT)人群中,基于独立影像评估委员会(IRRC)评估,信迪利单抗(达伯舒®)+贝伐珠单抗(达攸同®)联合化疗组(以下简称:双达联合化疗组)较标准化疗组在中位无进展生存(mPFS)方面获得显著且具有临床意义的延长( 7.2月 vs 4.3月,P<0.0001)。在次要终点客观缓解率(ORR)和缓解持续时间(DOR)上,双达联合化疗组较化疗组均有提高,与主要终点获益结论一致。安全性特征与既往报道的信迪利单抗、贝伐珠单抗相关临床研究结果一致,无新的安全性信号。 ORIENT-31研究的第一次期中分析结果已于2022年07月28日发表于《柳叶刀·肿瘤学》(The Lancet Oncology)1。第二次期中分析结果已于2023年5月5日发表于《柳叶刀·呼吸医学》(The Lancet Respiratory Medicine)2。 ORIENT-31研究的主要研究者 上海市胸科医院肿瘤科 陆舜 教授 与西方人群显著不同,我国约一半非鳞状非小细胞肺癌患者具有EGFR突变,尽管可从EGFR-TKI治疗中获益。但是,目前EGFR-TKI治疗进展后选择十分有限、疗效不令人满意,临床上迫切需要新的治疗选择3。ORIENT-31研究是全球首个证实PD-1抑制剂±贝伐珠单抗联合化疗能够显著延长EGFR-TKI治疗失败的EGFR突变非鳞NSCLC人群PFS的前瞻性、随机,双盲3期研究,具有划时代意义。此外,与标准含铂化疗相比,信迪利单抗和贝伐珠单抗联合化疗提高了患者客观缓解率、缓解持续时间,在显示生存获益趋势的同时,生活质量有一定程度的获益。该适应症获批为我国EGFR-TKI治疗失败的NSCLC患者带来全新治疗选择,极大惠及EGFR突变患者,改变现有治疗标准。 礼来中国总裁兼总经理 贝栎铭 先生 自2018年起,达伯舒®(信迪利单抗注射液)已连续获批包括鳞状及非鳞状非小细胞肺癌、肝细胞癌、胃腺癌、食管鳞癌、与经典型霍奇金淋巴瘤在内的6大适应症且均已被纳入国家医保目录,为中国数百万癌症患者带来福音。很高兴看到达伯舒®(信迪利单抗注射液)又一适应症的获批,实现了EGFR阳性非鳞状非小细胞肺癌免疫治疗领域的‘零突破’,为更多中国晚期EGFR-TKI治疗失败的EGFR突变非小细胞肺癌患者带来创新免疫治疗选择。达伯舒®(信迪利单抗注射液)是我们与本土领先的生物制药公司信达生物合作的最佳见证。未来,我们将继续探索多元化的合作模式,让更多的创新药物尽早惠及中国肿瘤患者,为擘画‘健康中国2030’的宏伟蓝图持续贡献力量。 礼来全球高级副总裁 礼来中国药物开发及医学事务中心负责人 王莉 博士 ORIENT-31研究是全球首个在EGFR阳性肺癌患者中证实有获益的免疫治疗的研究,截至目前两次期中分析均取得了令人可喜的临床结果,有望打破EGFR-TKI耐药困境,为经EGFR-TKI治疗失败的EGFR阳性非鳞状非小细胞肺癌患者提供全新的治疗选择。达伯舒®(信迪利单抗注射液)新适应症的获批,也为中国晚期EGFR-TKI治疗失败的EGFR突变的非小细胞肺癌患者带来新的生存希望。 信达生物制药创始人、董事长兼首席执行官 俞德超 博士 免疫治疗在驱动基因阳性的NSCLC患者上一直鲜有突破。然而,越是充满挑战,越需要知重负重、攻坚克难。信达生物秉承‘开发出老百姓用得起的高质量生物药’的使命,与中国患者、研究者携手完成ORIENT-31研究。达伯舒®联合贝伐珠单抗及化疗方案获批是目前我国首个批准用于EGFR阳性NSCLC患者的免疫联合疗法,信达生物将继续努力,深耕创新,为实现‘健康中国2030’添砖加瓦,为推进健康中国建设贡献‘信达力量’。 信达生物制药集团高级副总裁 周辉 博士 肺癌是我国死亡率最高、发病率最高的恶性肿瘤4,是我国面临的重大公共卫生问题,具有巨大的未满足临床需求。达伯舒®联合贝伐珠单抗及化疗用于经表皮生长因子受体酪氨酸激酶抑制(EGFR-TKI)治疗失败的EGFR突变非鳞状非小细胞肺癌适应症获批是本产品开发的又一重要里程碑,给广大EGFR突变的肺癌患者带来新的希望。信达生物将一如既往围绕未满足临床需求开展临床研究,为中国和全球患者带来更多有效的治疗选择。 关于ORIENT-31研究 ORIENT-31研究是一项比较达伯舒®(信迪利单抗注射液)联合或不联合贝伐珠单抗以及化疗用于经EGFR-TKI治疗进展的EGFR突变的局部晚期或转移性非鳞非小细胞肺癌患者的有效性和安全性的随机、双盲、多中心三期临床研究(ClinicalTrials.gov, NCT03802240)。主要研究终点为IRRC根据RECIST v1.1标准评估的无进展生存期,次要研究终点包括总生存期(OS)、研究者根据RECIST v1.1标准评估的无进展生存(PFS)、客观缓解率(ORR)和安全性等。 关于信迪利单抗 信迪利单抗,中国商品名为达伯舒®(信迪利单抗注射液),是信达生物制药和礼来制药共同合作研发的具有国际品质的创新PD-1抑制剂药物。信迪利单抗是一种人类免疫球蛋白G4(IgG4)单克隆抗体,能特异性结合T细胞表面的PD-1分子,从而阻断导致肿瘤免疫耐受的 PD-1/程序性死亡受体配体1(Programmed Death-Ligand 1, PD-L1)通路,重新激活淋巴细胞的抗肿瘤活性,从而达到治疗肿瘤的目的5。目前有超过二十多个临床研究(其中10多项是注册临床试验)正在进行,以评估信迪利单抗在各类实体肿瘤和血液肿瘤上的抗肿瘤作用。 信迪利单抗已在中国获批七项适应症,其中前六项纳入2022版国家医保目录,医保目录中描述的协议期内医保目录描述的限定支付范围包括: 不可切除的局部晚期、复发或转移性食管鳞癌的一线治疗; 不可切除的局部晚期、复发或转移性胃及胃食管交界处腺癌的一线治疗; 表皮生长因子受体(EGFR)基因突变阴性和间变性淋巴瘤激酶(ALK)阴性、不可手术切除的局部晚期或转移性非鳞状非小细胞肺癌(NSCLC)患者的一线治疗; 不可手术切除的局部晚期或转移性鳞状非小细胞肺癌(NSCLC)的一线治疗; 既往未接受过系统治疗的不可切除或转移性肝细胞癌的一线治疗; 至少经过二线系统化疗的复发或难治性经典型霍奇金淋巴瘤的治疗。 另外, 信迪利单抗已获批联合贝伐珠单抗、培美曲塞和顺铂,用于经表皮生长因子受体酪氨酸激酶抑制剂(EGFR-TKI)治疗失败的EGFR基因突变阳性的局部晚期或转移性非鳞状非小细胞肺癌(NSCLC)患者的治疗。 信迪利单抗另有两项临床试验达到研究终点,包括: 单药用于晚期/转移性食管鳞癌二线治疗的二期临床研究; 单药用于含铂化疗失败的晚期鳞状非小细胞肺癌二线治疗的三期临床研究。 声明:以上2项适应症尚未在中国大陆获批,礼来不推荐任何未获批的药品/适应症使用 关于礼来制药与信达生物的战略合作 礼来制药与信达生物于2015年3月达成了一项生物技术药物开发合作,该合作亦是迄今为止中国生物制药企业与跨国药企之间最大的合作之一。根据合作条款,信达生物和礼来制药将在中国共同开发和商业化包括达伯舒®(信迪利单抗注射液)在内的肿瘤药物。2015年10月,双方宣布再次拓展已建立的药物开发合作,增加三个新型肿瘤治疗抗体。2019年8月,双方合作扩展至糖尿病领域,信达生物获授权在中国开发和商业化礼来的一个潜在全球最佳新型临床阶段糖尿病药物。这三次与礼来制药的合作标志着信达生物已建立起一个由中国创新药企与全球制药巨头之间的全面战略合作,其范围涵盖新药研发,临床研究,生产质量和市场销售等。2020年8月,礼来制药与信达生物宣布扩大信迪利单抗的战略合作。2022年3月,礼来制药宣布深化与信达生物在肿瘤领域的战略合作,礼来授予信达生物希冉择®(雷莫西尤单抗)和睿妥®(塞普替尼)在中国大陆获批后独家商业化权利,以及授予信达生物享有Pirtobrutinib未来在中国大陆商业化权利的优先谈判权。 关于礼来制药 礼来制药是一家从事药品研发、生产和销售的全球领先的医药公司,致力于通过创新改善人类健康水平。礼来制药诞生于一个多世纪之前,于1876年由礼来上校在美国印第安纳州创立,公司创始人致力于生产高质量的药品以满足切实的医疗需求。今天,我们仍然执着于这一使命,并基于此开展工作。在全球范围内,我们的员工始终努力研发能为人类生活带来改变的药物,并将其提供给那些切实所需的患者。不仅如此,我们还致力于改善公众对于疾病的理解、并更好地开展疾病管理,同时通过投身于慈善事业和志愿者活动回馈社会。礼来本着“植根中国,造福中国”的理念,着力拓展在华业务,在糖尿病、肿瘤、免疫、疼痛和神经退行性疾病等领域居领先地位。如果需要了解更多关于礼来制药的信息,请登录:www.lilly.com。 关于信达生物 “始于信,达于行”,开发出老百姓用得起的高质量生物药,是信达生物的理想和目标。信达生物成立于2011年,致力于开发、生产和销售肿瘤、自身免疫、代谢、眼科等重大疾病领域的创新药物。2018年10月31日,信达生物制药在香港联合交易所有限公司主板上市,股票代码:01801。 自成立以来,公司凭借创新成果和国际化的运营模式在众多生物制药公司中脱颖而出。建立起了一条包括35个新药品种的产品链,覆盖肿瘤、自身免疫、代谢、眼科等多个疾病领域,其中7个品种入选国家“重大新药创制”专项。公司已有 8个产品(信迪利单抗注射液,商品名:达伯舒®,英文商标:TYVYT®;贝伐珠单抗生物类似药,商品名:达攸同®,英文商标:BYVASDA®;阿达木单抗生物类似药,商品名:苏立信®,英文商标:SULINNO®;利妥昔单抗生物类似药,商品名:达伯华®,英文商标:HALPRYZA®; 佩米替尼片,商品名:达伯坦®,英文商标:PEMAZYRE®; 奥雷巴替尼片,商品名:耐立克®; 雷莫西尤单抗,商品名:希冉择®,英文商标:CYRAMZA®;塞普替尼胶囊,商品名:睿妥®,英文商标:RETsevmo®)获得批准上市, 3个品种在NMPA审评中,5个新药分子进入III期或关键性临床研究,另外还有19个新药品种已进入临床研究。 信达生物已组建了一支具有国际先进水平的高端生物药开发、产业化人才团队,包括众多海归专家,并与美国礼来制药、赛诺菲、Adimab、Incyte和MD Anderson 癌症中心等国际合作方达成战略合作。信达生物希望和大家一起努力,提高中国生物制药产业的发展水平,以满足百姓用药可及性和人民对生命健康美好愿望的追求。详情请访问公司网站:www.innoventbio.com或公司领英账号www.linkedin.com/company/innovent-biologics/。 参考文献 1.Lu S, Wu L, Jian H, et al. Sintilimab plus Bevacizumab biosimilar IBI305 and chemotherapy for patients with EGFR-mutated non-squamous non-small-cell lung cancer who progressed on EGFR tyrosine-kinase inhibitor therapy (ORIENT-31): first interim results from a randomised, double-blind, multicentre, phase 3 trial.Lancet Oncol.2022;S1470-2045(22)00382-5.doi:10.1016/S1470-2045(22)00382-5. 2.Lu S, Lin, Wu, et al. Sintilimab plus chemotherapy for patients with EGFR-mutated non-squamous non-small-cell lung cancer with disease progression after EGFR tyrosine-kinase inhibitor therapy (ORIENT-31): second interim analysis from a double-blind, randomised, placebo-controlled, phase 3 trial. Lancet Respir Med May 5, 2023. doi:10.1016/S2213-2600(23)00135-2. 3.Chen P, Liu Y, Wen Y, et al. Non‐small cell lung cancer in China[J]. Cancer Communications, 2022, 42(10): 937-970. 4.Zheng R, Zhang S, Wang S, et al. Lung cancer incidence and mortality in China: updated statistics and an overview of temporal trends from 2000 to 2016[J]. Journal of the National Cancer Center, 2022. 5.Wang J, Fei K, Jing H, et al. Durable blockade of PD-1 signaling links preclinical efficacy of sintilimab to its clinical benefit. mAbs 2019;11(8): 1443-1451.